Pod względem naukowym w obszarze TPD dzieje się dużo dobrego, ale niekoniecznie to się przekłada na wyceny spółek - Michał Walczak i Radosław Krawczyk, Captor Therapeutics
Technologia TPD wciąż szybko się rozwija i zalicza kolejne postępy. Captor Therapeutics, polska spółka z tego sektora, jako jedna z nielicznych na świecie wciąż posiada pełnię praw do wszystkich swoich najbardziej zaawansowanych projektów. O obecnej sytuacji w spółce, postępie badań, rozliczeniach grantów i planowanej emisji akcji rozmawiam z Michałem Walczakiem, Dyrektorem Naukowym i Radosławem Krawczykiem, Dyrektorem Finansowym Captor Therapeutics.
Paweł Biedrzycki: Nastroje w polskiej biotechnologii się nieco poprawiły. Inwestorzy znowu zaczęli mocniej interesować się sektorem, udają się kolejne oferty SPO spółek z sektora. Czujecie, że atmosfera na GPW wokół sektora się poprawiła?
Michał Walczak: W pewnym sensie tak, ale z drugiej strony wyceny wciąż nie wróciły do poziomów sprzed kryzysu.
REKLAMA
Radosław Krawczyk: Zdecydowanie wyceny wciąż nie wróciły do dawnych poziomów, pomimo że kluczowe projekty poszły do przodu i wydaje się, że inwestorzy na GPW doskonale sobie z tego zdają sprawę. Obecne wyceny perspektywicznych spółek z sektora wydają się być interesujące. Najlepszym przykładem jest ostatnia oferta SPO Molecure. Z komunikatu, który opublikowała spółka po ofercie, wynika, że popyt przekroczył podaż, a mówimy o ofercie o wartości 50 mln zł. To jest bardzo budujące.
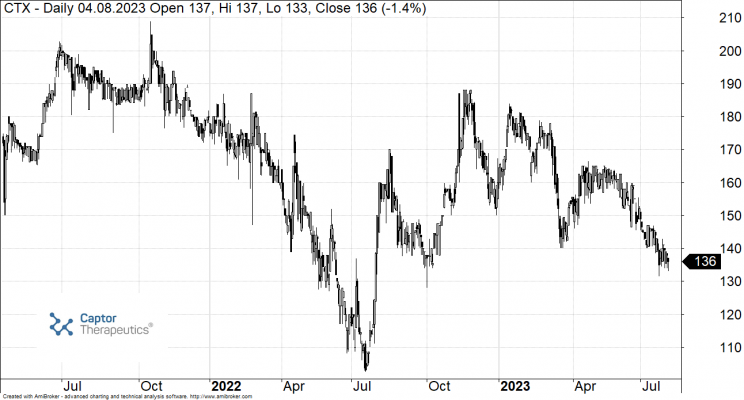
Notowania Captor Therapeutics
Trochę gorzej wygląda to, jeśli chodzi o sektor TPD na świecie. Jak skomentujecie presję rynkową jaka pojawiła się na takich spółkach jak Arvinas czy C4?
MW: Pod względem naukowym w obszarze TPD dzieje się dużo dobrego, ale niekoniecznie to się przekłada na wyceny spółek. W tej chwili w USA ma miejsce taka sytuacja, że wiele spółek z tego obszaru jest wycenianych na poziomie gotówki na kontach. Jest to pochodna trzech kwestii. Z jednej strony wiele spółek z tego sektora weszło w fazy kliniczne swoich badań i koszty tych badań są znacząco wyższe od faz przedklinicznych, a co ciekawe większość tych spółek jest już po komercjalizacjach i nie mają za bardzo czego sprzedawać, aby pozyskać kolejne środki. Jednocześnie nie mogą liczyć na wsparcie grantowe w takim zakresie, jakie chociażby my posiadamy. Trzecią kwestią jest - niestety - jakość niektórych projektów. Tutaj przykładem może być chociażby C4 Therapeutics, które odnotowało poważne problemy i w pierwszym, i drugim swoim najbardziej zaawansowanym projekcie, co poważnie nadszarpnęło zaufanie inwestorów.
Zobacz także: Kraje regionu zazdroszczą nam rozwoju polskiej biotechnologii - Paweł Przewięźlikowski Ryvu Therapeutics, Podcast "21% rocznie"
Co ważnego od początku roku wydarzyło się w takim razie pod względem naukowym w obszarze TPD?
MW: Spektakularnych wyników naukowych w ostatnich miesiącach nie było, bo nie było też odczytów wyników z badań klinicznych. Z mojej perspektywy zwróciłbym uwagę na wyniki Celgene dla związku CC-92480, gdzie okazało się, że klej molekularny opracowany przez spółkę degraduje nie jedno, ale dwa białka. Publikacja naukowa pokazała, że degradacja drugiego białka, ZFP91, jest kluczowa w pokonaniu oporności w nowotworach szpiczaka. Na podstawie tych badań upatruję dużego potencjału w naszych klejach molekularnych z projektu CT-01. Arvinas natomiast przedstawił drugą generację PROTACa, które są w stanie przełamywać oporność nowotworów w leczeniu raka prostaty. Oporność ta jest ukierunkowana wobec niektórych klasycznych leków i wynika z mutacji w celu molekularnym, receptorze androgenu. W tym roku Kymera wprowadziła do fazy klinicznej swój degrader bispecyficzny celujący w bardzo uznany w biotechnologii cel molekularny, jakim jest białko MDM2. Śledzimy ten projekt, ponieważ dopatrujemy się podobnego mechanizmu działania w naszym projekcie dotyczącym MCL-1. Mechanizm ten w tych konkretnych przypadkach pozwala na pokonanie farmakologicznych ograniczeń klasycznych inhibitorów i rozszerzenie okna terapeutycznego. W sektorze dzieje się naprawdę dużo i widać, że rozwój TPD postępuje.
Czy zaobserwowaliście jakieś wydarzenia, które wpływałyby na wasz pipeline badawczy, zwłaszcza projekty, które weszły w obszary, które Wy staracie się zaadresować?
MW: Nic nas szczególnie negatywnie nie zaskoczyło. Z branżowego punktu widzenia negatywnie na postrzeganie sektora mogą wpływać problemy C4 Therapeutics. Ewidentnie spółka ma w swoich badaniach „pecha”, ale z drugiej strony ich historia uwydatnia to, czego my mieliśmy świadomość od samego początku. Nie zawsze jest sens w rozwijaniu projektów TPD, gdzie dobrze działają inhibitory. Chyba, że ograniczenia inhibitorów w tych obszarach są dobrze poznane.
Jak wyglądają postępy w Waszym pipelinie badawczym. Może zacznijmy od waszej współpracy z ONO czy Sosei, czy widać tutaj jakieś postępy i jakie są możliwe dalsze kierunki współpracy?
MW: Jesteśmy bardzo zadowoleni ze współpracy z Sosei. Pierwotnie miała ona trwać dwa lata, a została przedłużona o pół roku. Jesteśmy na ostatniej prostej kończącej wszystkie zaplanowane badania. Będziemy mieli jeszcze spotkanie podsumowujące całą współpracę, w trakcie którego zapewne zostanie podjęta decyzja co dalej. Jeśli chodzi o ONO, to współpraca jest na wcześniejszym etapie, ale rozwija się bardzo dobrze. Mieliśmy wizytę przedstawicieli wysokiego szczebla reprezentujących korporację we Wrocławiu, wkrótce my wybieramy się do Japonii. Na ten moment mogę jedynie powiedzieć, że potencjał współpracy może być większy niż nam się na początku wydawało.
Zobacz także: Sztuczna inteligencja, ożywienie na rynku i nowe terapie. Nowe trendy w sektorze biotechnologicznym oczami polskich spółek po BIO Convention Boston
Na początku roku zapowiadaliście, że przewidujecie, że w tym roku Captor stanie się spółką kliniczną. Jak wyglądają postępy w Waszych kluczowych projektach, zwłaszcza w CT-01?
MW: Jesteśmy już na etapie przygotowywania wniosku, który trzeba złożyć przed rozpoczęciem badań. Podtrzymujemy to, że w 2023 roku chcemy się stać spółką w fazie klinicznej, którym będzie CT-01. Jesteśmy też bardzo zadowoleni z projektu CT-03. Tutaj udało nam się zsyntetyzować kilogram związku, który jest bardzo aktywny. W tym projekcie również jesteśmy coraz bliżej fazy klinicznej badań. CT-02 również wygląda bardzo obiecująco, jeśli chodzi o nasz pipeline. O związku było ostatnio głośno za sprawą całego zamieszania z NCBiR, ale pomijając kwestie formalne, tutaj wyniki badań okazały się bardzo obiecujące i projekt ma olbrzymi potencjał w leczeniu chorób neurodegeneracyjnych, jak Parkinson czy Alzheimer, nie wspominając nawet całej listy chorób autoimmunologicznych poza Ośrodkowym Układem Nerwowym. Liczymy, że to może być czarny koń całego naszego portfela projektów.
Związki TPD charakteryzują się tym, że są bardzo aktywne. Do osiągnięcia efektu potrzebne są zazwyczaj dużo mniejsze dawki niż w terapiach celowanych czy immunoonkologii. Jak to w praktyce będzie wpływać zwłaszcza na 1 fazę kliniczną badań?
MW: Badanie pierwszej fazy planujemy rozpocząć na osobach chorych głównie w Niemczech i Francji. To wynika z faktu, że mamy dobrze rozpoznany pod tym względem obszar w tych krajach i powinniśmy szybko zrekrutować pacjentów. Substancja jaką będą otrzymywać pacjenci jest bardzo aktywna, dlatego dawki będą niezwykle niskie, na początku być może nawet poniżej 1 mg na pacjenta. To oczywiście z jednej strony jest wielkim plusem, bo zmniejsza prawdopodobieństwo toksyczności, ale z drugiej strony wyzwaniem, bo w jakiś sposób trzeba umieścić tak małą ilość aktywnej substancji w tabletce. Pracujemy teraz nad końcową formą leku w tabletce z uznanym dostawcą takich rozwiązań. Granty.
Dużo się u was dzieje pod tym względem. Z jednej strony mamy nowo pozyskane granty a ABM, a z drugiej problemy z rozliczeniem jednego z projektów z NCBiR. Czy pod względem finansowym czujecie się obecnie komfortowo?
MW: Czujemy się bardzo dobrze, ale przerwanie naszego grantu, który był dedykowany projektowi CT-02, oczywiście nie jest dobrą wiadomością. Pierwsze dwie części badań nad tym projektem mieliśmy zatwierdzone i rozliczone, a w trakcie trzeciej zawnioskowaliśmy o pewne zmiany, które polegały na rozszerzeniu prac, a które ostatecznie nie zostały zaakceptowane przez NCBiR. Podtrzymujemy nasze stanowisko o braku uzasadnienia zastosowania wskazanych przez NCBiR podstaw rozwiązania umowy oraz uważamy, że żądanie zwrotu całości otrzymanego dofinansowania jest nadmiarowe i pozbawione uzasadnienia.
Czy to jedyny projekt, w którym wystąpiła taka zmiana, bez wcześniejszego zatwierdzenia przez NCBiR?
MW: Wszystkie inne projekty prowadzone są zgodnie z harmonogramem i tym, co zatwierdził NCBiR, dlatego nie widzimy podstaw, aby były one w jakikolwiek sposób zagrożone. Zamykając temat CT-02 - chcę jedynie dodać, że wprowadzone zmiany były efektem uzyskania ekscytujących wyników badań z wcześniejszych etapów, które miały na celu zwiększyć prawdopodobieństwo sukcesu. Jesteśmy zadowoleni z dalszych postępów tego projektu i zamierzamy kontynuować prace nad nim, nawet pomimo braku finansowania grantowego.
Zobacz także: Liczymy, że w 2023 Captor Therapeutics stanie się spółką TPD z projektem w fazie klinicznej co znacznie zmieni postrzeganie naszej firmy - Michał Walczak i Radosław Krawczyk
Captor Therapeutics jest w stanie pozyskiwać dalsze granty?
MW: Jesteśmy w stanie i pozyskujemy. Właśnie otrzymaliśmy grand od ABM w wysokości 52 mln zł na niezwykle ciekawy projekt, który celuje w białko niedostępne (ang. Undruggable) dla inhibitorów. Ubiegamy się obecnie o kolejne finansowania, tym razem z PARP.
RK: Pomimo tego potknięcia pozostajemy w świetnych relacjach z NCBiR jako jeden z kluczowych beneficjentów ich środków w obszarze drug discovery. Do tej pory zawarliśmy umowy dotyczące dofinansowania ok. 170 mln zł finansowania, wszystkie nasze projekty były bardzo wysoko oceniane i będziemy się ubiegać o kolejne.
W tym roku uchwaliliście kapitał docelowy. Czy pracują nad ofertą jakie są możliwe scenariusze pozyskania kapitału?
RK: W tym obszarze pracujemy zgodnie ze strategią. Podtrzymujemy, że w średnim terminie chcemy pozyskać inwestora strategicznego, najlepiej ze Stanów Zjednoczonych. Kapitał docelowy została uchwalona na trzy lata, więc mamy jeszcze trochę czasu. Pracujemy obecnie z bankiem inwestycyjnym Wedbush nad wyborem odpowiedniego momentu transakcji. Sytuacja w USA wciąż nie sprzyja pozyskiwaniu kapitału, aczkolwiek powoli się poprawia. Strategia jest dla nas punktem wyjścia, ale pozostajemy oczywiście elastyczni i gotowi podjąć najlepszą decyzję na drodze do budowania wartości Captora, dlatego nie zamykamy się na polskich inwestorów i rozważamy wszystkie opcje.
Rozmowy z potencjalnymi partnerami i strategia komercjalizacji. Czy pojawiły się nowe kierunki co w tej chwili wygląda najbardziej obiecująco?
RK: Tutaj również pracujemy zgodnie ze strategią. Projekty CT-01 i CT-03 planujemy rozwijać w pierwszej fazie samodzielnie i dopiero je komercjalizować po jej zakończeniu, a jeśli chodzi o projekt CT-02, to planujemy rozpocząć rozmowy komercjalizacyjne w drugiej połowie tego roku.