Genomtec pracuje nad urządzeniem Genomtec ID już dwa lata. System jest w początkowej fazie industrializacji
Genomtec jest pionierem w opracowaniu pierwszych w Polsce testów na wirusa SARS-CoV-2 w technologii izotermalnej - Genomtec® SARS-CoV-2 RT-LAMP / N CE-IVD. Ultraszybkie testy wprowadzone do sprzedaży w czerwcu br. przeznaczone są dla laboratoriów do szybkiej identyfikacji genetycznej wirusa wywołującego COVID-19. Obecnie Spółka pracuje nad flagowym projektem mobilnego urządzenia do diagnostyki molekularnej Genomtec ID.
Genomtec
Genomtec to polska firma biotechnologiczna specjalizująca się w innowacyjnym opracowaniu i komercjalizacji mobilnego systemu do diagnozy klinicznej różnych chorób zakaźnych, w tym testów Genomtec® SARS-CoV-2 RT-LAMP / N CE-IVD, które przeznaczone są do szybkiej identyfikacji genetycznej wirusa.
REKLAMA
„Opracowane i wprowadzone do sprzedaży w czerwcu br. testy diagnostyczne Genomtec® Genomtec® SARS-CoV-2 RT-LAMP / N CE-IVD przeznaczone dla laboratoriów do szybkiej identyfikacji genetycznej wirusa SARS-CoV-2 zostały formalnie dopuszczone do sprzedaży w Europie oraz mogą być dystrybuowane na innych kontynentach. Genomtec ma podpisane umowy dystrybucyjne w celu globalnej sprzedaży testów. Ceny testów są konkurencyjne wobec zestawów w starszej i wolniejszej technice PCR, zaś dostępne są na zapytanie ofertowe i uzależnione od wolumenu dostaw do poszczególnego klienta. Co więcej, zestawy diagnostyczne są nadal usprawniane, czego efektem jest niedawne zwalidowanie testu do wykorzystania z próbkami śliny, które z powodzeniem mogą zastąpić uciążliwe w pobieraniu wymazy, np. z nosa lub gardła. Opracowanie testów diagnostycznych pozwala na realizację przychodów ze sprzedaży, które będą również jednym ze źródeł finansowania prac B+R” - mówi Miron Tokarski, prezes, CEO i współzałożyciel Genomtec.
Ponadto, obecnie firma posiada opracowane testy w kierunku detekcji 8 patogenów, z których cztery posiadają już zgłoszenia patentowe. Poza SARS-CoV-2, opracowane zestawy testowe pozwalają na diagnozę HPV (wirus brodawczaka ludzkiego) najbardziej onkogenne typy ponadto bakterii odpowiadających często za atypowe zapalenie płuc u dzieci, a także bakterii Borrelia burgdorferi, która powoduje boreliozę. Docelowo portfolio wzbogacone zostanie o kolejne zestawy testowe, które tworzyć będą kompletne panele diagnostyczne np. w kierunku atypowych zakażeń dróg oddechowych.
Genomtec ID to urządzenie, dzięki któremu będzie można szybko i precyzyjnie wykonywać analizę genetyczną poza laboratorium bez konieczności wykwalifikowanego personelu laboratoryjnego. Urządzenie wykorzystuje technologię mikro przepływową, a także technologię izotermalną SNAAT® chronioną patentem. Spółka na ten projekt uzyskała dofinansowanie od NCBiR w wysokości ok. 7 mln złotych. Wygląd urządzenia przypomina niewielki sześcian mieszczący się w dłoni, który pozwoli na szybkie przeprowadzenie testu genetycznego m.in. w diagnostyce infekcji dróg oddechowych, w tym na COVID-19 nawet w 15 minut. System ma być przeznaczony do diagnostyki w miejscach takich jak gabinety gabinety lekarskie, w czasie wizyt domowych, transportu do szpitala czy pokój konsultacji aptek. Sam proces produkcji urządzenia będzie przebiegał w ścisłej współpracy z międzynarodową firmą typu CMO(ang. Contract Manufacturing Organization). Komercjalizacja urządzenia Genomtec ID ma nastąpić w I półroczu 2022 roku.
Zobacz także: Genomtec prezentuje swoje flagowe rozwiązanie
Testy PCR
Technika PCR z ang. Polymerase Chain Reaction to reakcja łańcuchowa polimerazy wykorzystywana do genetycznej diagnostyki medycznej. PCR została opracowana przez Kary’ego Mullisa w 1983 roku, za którą otrzymał Nagrodę Nobla w roku 1993. Technika ta pozwala na analizę materiału genetycznego DNA, a po połączeniu jej z reakcją nazywaną odwrotną transkrypcją ( z ang. Reverse transcription; skrót RT), jak również RNA, o niewielkim stężeniu wyjściowym, takim jakie jest uzyskiwane przy wymazie z gardła, przy rozpoznawaniu chorób zakaźnych układu oddechowego.
Reakcja diagnostyczna w technice PCR wykrywa specyficzny fragment kwasu nukleinowego, czyli DNA lub RNA, który należy do patogenu, na przykład bakterii czy wirusa, jak również mutacji obecnej w tkance człowieka. Proces ten odbywa się poprzez wielokrotne namnożenia tego fragmentu w reakcji enzymatycznej z wykorzystaniem polimerazy i w metodzie przebiegającej z odczytem sygnału w czasie rzeczywistym przez przyłączenie do powielonego fragmentu specjalnego barwnika molekularnego lub tzw. sondy molekularnej, umożliwiających powstanie sygnału(fluorescencyjnego), który jest następnie sczytywany przez specjalistyczne urządzenie diagnostyczne, czyli termocykler Real-Time PCR. Przy wykorzystaniu odpowiednich standardów kwasu nukleinowego o znanym stężeniu analizowanych łącznie z badanymi próbkami pozwala ona na określenie ilości kopii patogenu w badanym materiale. Do przeprowadzenia reakcji Real-Time PCR, oprócz barwnika i enzymu (polimerazy), potrzebne są również m.in. syntetyczne fragmenty DNA, których sekwencja jest wypadową sekwencji materiału genetycznego patogenu, którego specyficzny fragment ma zostać wykryty.
Mamy dwa startery dla każdego poszukiwanego fragmentu DNA w reakcji Real-Time PCR. Rozpoznanie celu na DNA należącym do patogenu odbywa się w ciekłej mieszaninie zwykle o objętości z przedziału 10-25 mikrolitrów (0,01-0,025 ml), którą zwyczajowo określa się jako „reakcyjną”, zawierającą również pozostałe składniki wykorzystywane do syntezy nowych odcinków kwasu nukleinowego. Całość tego procesu odbywa się na różnych etapach temperaturowych. Pierwszy etap to rozplecenie podwójnej helisy DNA, czyli tak zwana denaturacja (95oC). Drugi to przyłączenie starterów do specyficznych miejsc na poszukiwanym fragmencie DNA patogenu, czyli tak zwana hybrydyzacja (45o – 60oC). Trzeci etap, czyli ostatni to wydłużanie/synteza nowej nici DNA, czyli tak zwana elongacja (72oC), przez kompleks polimerazy ze starterami, oraz „wbudowanie” do nowo zsyntetyzowanego DNA barwnika molekularnego.
„Trzy powyżej wymienione etapy temperaturowe składają się na całość cyklu i muszą następować po sobie w ściśle ustalonej sekwencji, a takich cykli zazwyczaj występuje od 35 do 40 podczas jednej reakcji PCR. Jest to niezbędne, aby móc poprawnie odczytać powstały sygnał (fluorescencyjny). Każdy z tych etapów temperaturowych zabiera określony czas,” np.: denaturacja pomiędzy 10 a 20 sekund, a łącznie hybrydyzacja oraz elongacja około 50 sekund” - czytamy w dokumencie informacyjnym.
Etapy te wymagają różnych, ale bardzo dokładnych temperatur, więc urządzenie (Real-Time PCR) musi w bardzo efektywny sposób grzać i chłodzić mieszaninę reakcyjną (zawartą w probówkach), dlatego też do samych czasów długości poszczególnych etapów termicznych trzeba doliczyć czas potrzebny na ogrzewanie i/lub chłodzenie mieszaniny reakcyjnej. Nie jest to bez znaczenia, ponieważ do całości trwania cyklów PCR musi zostać dodane przynajmniej 15 minut (na wysokiej klasy urządzeniu Real-Time PCR).
„Jeżeli naszym celem diagnostycznym jest patogen, którego kwas nukleinowy występuje w formie RNA, jak w przypadku wirusa SARS-CoV-2 czy wirusa powszechnej grypy, przed opisywanym procesem denaturacji, hybrydyzacji oraz elongacji DNA, kwas RNA musi zostać „przepisany” we wspomnianej wcześniej reakcji odwrotnej transkrypcji na komplementarny DNA (cDNA), z udziałem dodatkowego enzymu –odwrotnej transkryptazy. Ten etap zajmuje kolejne 10 do 30 minut przed opisywanymi 40 cyklami syntezy specyficznego fragmentu DNA. Średni czas wykonania reakcji Real-Time PCR na obecność patogenu, którego kod genetyczny występuje w formie kwasu nukleinowego RNA, zajmuje około 80 minut, a często nawet dłużej, w zależności od jakości użytych enzymów i sprawności urządzenia Real-Time PCR (jego systemów optycznych oraz grzania i chłodzenia)” - czytamy dalej w dokumencie informacyjnym.
Zobacz także: Genomtec otrzymał dofinansowanie z NCBiR na dostosowanie mobilnego systemu do diagnostyki molekularnej
Testy LAMP od Genomtec
LAMP z ang. Loop Medicated Isothermal Nucleic Acid Amplification to technika amplifikacji kwasów nukleinowych w warunkach izotermalnych zachodząca w stałej temperaturze. Technika ta jest o wiele młodsza od reakcji PCR. Jej najbardziej wyjątkowa odmiana została opracowana przez japoński zespół Natomi w 1998 roku. Nowatorskość tej techniki leży nie tylko w jej izotermalnym przebiegu, czyli w warunkach zachodzących w stałej temperaturze, ale również przez zniwelowanie wymogu grzania i chłodzenia mieszaniny reakcyjnej.
„W technice LAMP startery rozpoznają komplementarne miejsca kwasu nukleinowego patogenu w bardzo podobnej temperaturze w jakiej działa sam enzym, dlatego samy etap hybrydyzacji oraz elongacji występują jednocześnie, bez potrzeby zmiany temperatury. Idąc dalej tropem „efektywności czasowej” techniki LAMP, używany w tej reakcji specjalny enzym posiadają podwójną funkcję, łącząc w sobie właściwości odwrotnej transkryptazy z funkcją polimerazy DNA, dlatego też w przypadku patogenów z informacją genetyczna kodowaną przez kwas RNA – jak w przypadku wirusa SARS-CoV-2, etapy odwrotnej transkrypcji i elongacji DNA zachodzą jednocześnie.”- czytamy w dokumencie informacyjnym.
Etap denaturacji jest tutaj przeprowadzany w formie tzw. inwazji startera na nić DNA (starter wykazując duże powinowactwo do specyficznego fragmentu matrycy DNA powoduje jej rozdzielenie, które jest wspomagane środowiskiem reakcji) oraz na drodze enzymatycznej, a nie jak w przypadku PCR poprzez wysoką temperaturę. Technika pozwala na zaoszczędzenie czasu podczas analizy próbki klinicznej pacjenta, ponieważ stała temperatura reakcji nie potrzebuje dodatkowego czasu na grzanie i chłodzenie mieszaniny reakcyjnej, a denaturacja zachodzi jednoczenie z syntezą cDNA, a w reakcji odwrotnej transkrypcji, zachodzi jednocześnie namnażanie wybranego fragmentu kwasu nukleinowego patogenu zachodzi jednocześnie z jrgo transkrypcją. Brak cykli temperaturowych pozwala na ciągłość pracy starterów w środowisku reakcji, dlatego też sygnał (fluorescencji) reakcji pojawia się znacznie szybciej.
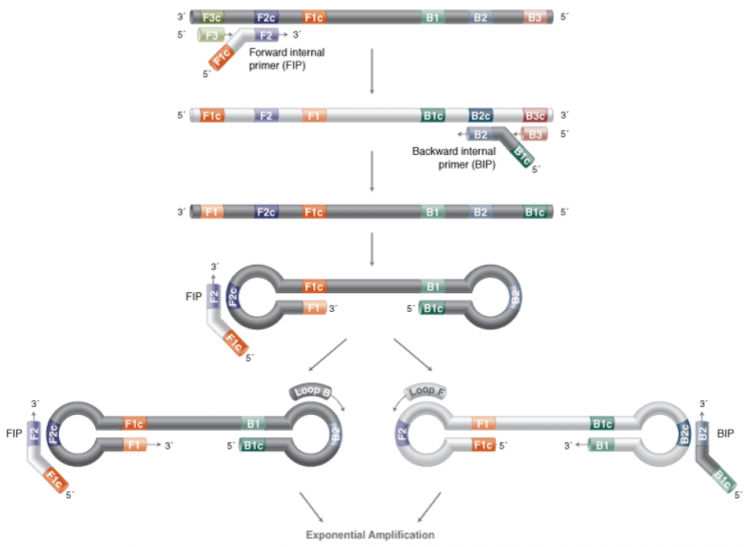
Schemat amplifikacji LAMP
Źródło: international.neb.com
W przypadku przeprowadzania procesu najczęściej wykorzystywana jest para starterów wewnętrznych tzw. „internal primers” - FIP i BIP, para zewnętrzna tzw. „out primers” – F3 i B3, a także dodatkowo stosowana jest para starterów zapętlających tzw. „loop primers”. Inne startery poza FIP i BIP służą do flankowania regionów amplifikacyjnych fragmentu kwasu nukleinowego. F3 i B3 są krótsze i występują w mieszaninie reakcyjnej w mniejszym stężeniu, tak aby ich wiązanie z matrycą było wolniejsze niż starterów wewnętrznych i inicjowały zastępowanie nici dupleksu przez nowo syntezowaną nić potomną.
Startery zewnętrzne mają za zadanie przemieszczenie nici, a startery wewnętrzne zawierają zarówno fragment komplementarny do nici sensownej jak i antysensownej pozwalając na tworzenie pętli. Dodatkowo stosowane startery zapętlające loop primers, które są komplementarne do regionów z uformowaną pętlą oraz zwiększają wydajność syntezy wybranego fragmentu kwasu nukleinowego, przez co skracają czas elongacji. Dzięki tym starterom, szybkość reakcji jest zwiększona poprzez wiązanie się do fragmentów docelowej sekwencji nie objętych przez startery wewnętrzne, w ten sposób cała amplifikacja przebiega szybciej (komplementarne DNA; cDNA).
Zobacz także: INC rozpoczyna współpracę z Genomtec i zapowiada kolejne debiuty na NewConnect
Testy PCR vs LAMP
Po porównaniu metod PCR i Lamp widać jednoznacznie, że amplifikacja izotermiczna wykazuje większą czułość niż reakcji łańcuchowa polimerazy. Co więcej, technika namnażania kwasu nukleinowego zachodzi w szybszy sposób, czyli od 10 do 30 minut, w porównaniu do ok. 80 minut w PCR. Zakres zastosowania LAMP został poszerzony poprzez połączenie metody z procesem odwrotnej transkrypcji (RT-LAMP -Reverse Transcription Loop-Mediated Isothermal Amplification), dzięki czemu możliwa jest detekcja wirusów RNA, z czułością większą niż w klasycznym RT-PCR. Również drugi parametr odgrywa kluczową rolę w diagnostyce – specyficznie jest wyższy w przypadku amplifikacji izotermicznej.
„Dzięki swoim unikatowym cechom technika ta doskonale sprawdza się także w urządzeniach przeznaczonych do wykorzystania w miejscu opieki nad pacjentem – POCT. Dzięki jednotemperaturowej reakcji możliwe jest zmniejszenie wymiarów urządzenia, zmniejszenie zużycia energii oraz kosztu zakupu – tak ważnych parametrów w diagnostyce rozproszonej. Genomtec aktualnie rozwija swoją technologie SNAAT®, oparta na technice LAMP, w swojej flagowej mobilnej platformie genetycznej – Genomtec ID, przeznaczonej do diagnostyki klinicznej pacjenta w systemie POCT” - czytamy w dokumencie informacyjnym.
Pomimo oczywistych przewag funkcjonalnych technologii LAMP nad PCR, jest ona procesem złożonym, wymagającym od osób odpowiedzialnych za opracowanie zestawów testowych doświadczenia w jej wykorzystaniu. Jednak obecna pandemia wywołująca chorobę COVID-19 zwróciła uwagę na niebanalne zalety LAMP, w szczególności w sytuacji braków kadrowych, ograniczonej ilości wyspecjalizowanych laboratoriów genetycznych oraz narastającej liczby pacjentów, których diagnostyka powinna odbywać się tylko z zastosowaniem testu genetycznego.
Ograniczenia związane z techniką PCR powodują, że diagnostyka genetyczna choroby COVID-19 staje się niewydolna, ponieważ zajmuje za dużo czasu. Opracowany dla danego patogenu test w technice LAMP, pokazuje swoje korzyści w prostszym i szybszym procesie diagnostycznym w którym jest wykorzystywany. Technik izotermalne, w tym LAMP, zyskują coraz większa popularność w stosowaniu w szybkich testach genetycznych do celów walki z pandemią COVID-19.
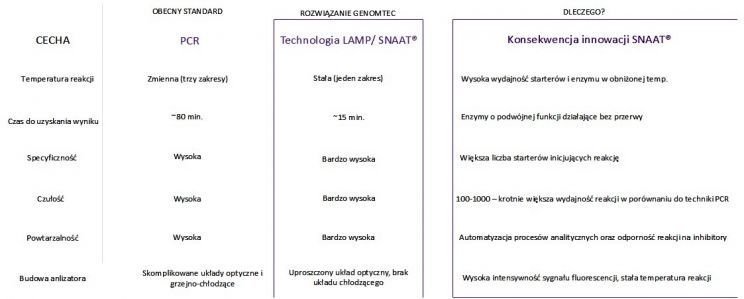
Porównanie testu PCR i testu Genomtec LAMP/SNAAT
Źródło: Genomtec
Firma Genomtec poinformowała na początku września, że planuje do końca roku zadebiutować na NewConnect. Jednakże docelowo chce być notowana na głównym parkiecie GPW.