Pure Biologics optymalizuje plan rozwoju swoich dwóch najbardziej zaawansowanych projektów lekowych i rozpoczyna intensyfikacje działań komercjalizacyjnych
Pure Biologics planuje zoptymalizować rozwój swoich dwóch najbardziej zaawansowanych projektów innowacyjnych cząsteczek PB003 i PB004. Spółka przedstawiła plan rozwoju projektów jednocześnie, co pozwoli przyspieszyć prowadzone nad nimi badania i zoptymalizować liczne koszty związane z rozwojem.
Pure Biologics, innowacyjna firma biotechnologiczna dysponująca własnymi platformami do wyszukiwania nowych leków biologicznych oraz tworząca terapie pozaustrojowe oparte o aptamery, przedstawiła plan optymalizujący rozwój projektów. Równoległy rozwój obu projektów pozwoli zoptymalizować liczne koszty związane z badaniem tych cząsteczek oraz pomoże w przyspieszeniu prac. Jednocześnie spółka intensyfikuje działania skierowane na licencjonowanie jednego z projektów.
REKLAMA
Zarówno w przypadku PB004, jak również w projekcie PB003 Pure planuje przeprowadzić fazę 0, która pozwoli nawet o dwa lata szybciej, niż w przypadku klasycznego podejścia, opartego na fazie I i II badań klinicznych, uzyskać pierwsze informacje o efektywności związków u ludzi. Pozyskanie danych w ten sposób nastąpi przy znacząco niższych, niż w przypadku klasycznego podejścia, nakładach finansowych.
„PB003 i PB004 to kluczowe spośród naszych projektów lekowych. Opracowaliśmy dla nich zsynchronizowany plan rozwoju, dzięki któremu planujemy obniżyć koszty wykonania części badań, a także przyspieszyć część procesów. Zdecydowaliśmy również, że w przypadku PB003 – podobnie jak w PB004 – będziemy chcieli przeprowadzić fazę 0 w ramach wspólnego badania, które już na wczesnym etapie rozwoju klinicznego da nam pierwsze wyniki efektywności naszych cząsteczek na ludziach. Zabezpieczamy finansowanie grantowe tych projektów oraz intensyfikujemy poszukiwanie partnera do jednego z naszych projektów. Taki plan rozwoju pomoże nam szybciej pozyskać partnera i uzyskać lepsze warunki w potencjalnej transakcji” – komentuje dr Filip Jeleń, współzałożyciel, istotny akcjonariusz i prezes zarządu Pure Biologics.
Wszystkie działania mają na celu znacząco przyspieszyć wzrost wartości projektów z punktu widzenia przyszłego partneringu oraz uzyskać istotną przewagę konkurencyjną. Rozpoczęcie fazy 0 w obu projektach ma być możliwe już w IV kw. 2023 r.
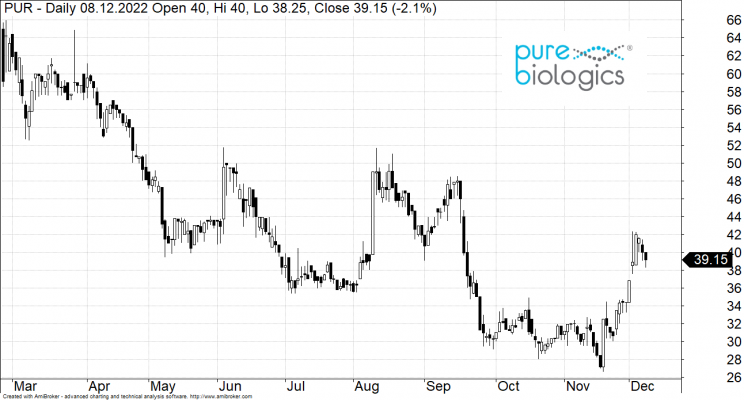
Kurs akcji Pure Biologics
Zobacz także: Emisja akcji Ryvu Therapeutics. Co warto wiedzieć o ofercie i planach spółki
Przyspieszenia działań nastawionych na poszukiwanie partnera
Oprócz optymalizacji planów rozwoju leków, spółka planuje przyspieszyć proces poszukiwania partnera. To efekt nawiązanej w tym roku współpracy z renomowanym doradcą w tym zakresie, Destum Partners. Spółka przyspiesza procesy związane z poszukiwaniem nabywcy na jeden z projektów spółki oraz intensyfikuje własne działania zorientowane na rozwój biznesu, przede wszystkim udział w międzynarodowych konferencjach branżowych i naukowych.
W ostatnim czasie projekt PB004 zagwarantował sobie dofinansowanie grantowe (dotacje na rozwój przedkliniczny i kliniczny z Narodowego Centrum Badań i Rozwoju (NCBR) i Agencji Badań Medycznych (ABM)), które obejmie rozwój cząsteczki aż do zakończenia I fazy badań klinicznych, i podejmuje działania celem zabezpieczenia podobnego finansowania w przypadku PB003. Tylko w przypadku dotacji z ABM, wartość dofinansowania może wynieść 32,4 mln zł.
Zarówno w projekcie PB003, jak i PB004, w 2022 r. rozpoczęły się badania in vivo. Prowadzone są one przez renomowanego, amerykańskiego wykonawcę - Jackson Laboratories – posiadającego duże doświadczenie w projektach immunoonkologicznych.
Zobacz także: Polska biotechnologia jest wciąż na wczesnym etapie rozwoju i najlepsze ma przed sobą – mówią uczestnicy BIOTECH DAY na GPW
Projekt PB004, potencjalny lek biologiczny, dotyczy rozwoju nowej cząsteczki terapeutycznej w formacie nieklasycznego przeciwciała, które ma stymulować odpowiedź immunologiczną komórek NK wobec komórek guza posiadających antygen nowotworowy ROR-1, prowadząc do bezpośredniego ich zabijania na drodze mechanizmu ADCC (ang. antibody-dependent cellular cytotoxicity). Cząsteczka PB004 rozwijana jest w kierunku leczenia guzów litych, w tym potrójnie negatywnego raka piersi, jak również w kierunku leczenia wybranych nowotworów hematologicznych, w tym m.in. przewlekłej białaczki limfocytowej.
We wrześniu spółka poinformowała o uzyskaniu od NCBR zgody na zmianę zakresu, harmonogramu i budżetu projektu. Zgodnie z podpisanym aneksem, koszty w projekcie spadną z 40,4 do 38,6 mln zł, a wkład własny spółki zostanie zredukowany o ponad 0,7 mln zł. Zmieniony harmonogram zakłada przeprowadzenie w projekcie tzw. „fazy 0”, polegającej na podaniu pacjentom mikrodawek kandydata na lek bezpośrednio do guzów nowotworowych, co pozwoli potwierdzić mechanizm działania cząsteczki w złożonym mikrośrodowisku guza oraz lepiej oszacować potencjalną skuteczność kandydata na lek w terapii przeciwnowotworowej.
W drugiej połowie listopada spółka poinformowała o uzyskaniu pozytywnej rekomendacji do dofinansowania projektu w konkursie ABM. Dotacja obejmuje dofinansowanie rozwoju przedklinicznego oraz fazy I badań klinicznych. Wartość dofinansowania wynosi 32,4 mln zł przy całkowitej wartości projektu na poziomie 50 mln zł. Pozyskane z tego źródła środki są komplementarne do już zabezpieczonego finansowania i pozwalają w sposób płynny na kontynuację rozwoju i przejście z fazy 0 do fazy I.
Projekt PB003, również potencjalny lek biologiczny, ma na celu opracowanie przeciwciała terapeutycznego o podwójnym działaniu, które jednocześnie eliminuje immunosupresyjne regulatorowe limfocyty T (Treg) w mikrośrodowisku guza oraz stymuluje cytotoksyczne limfocyty NK i T do bezpośredniego zwalczania komórek nowotworowych. Proponowane w ramach projektu PB003 podejście terapeutyczne posiada wyraźne przewagi w stosunku do kandydatów na leki z obiecującymi wynikami we wczesnych etapach rozwoju klinicznego dla dwóch niezależnie rozwijanych w tym projekcie kandydatów na leki (PB003A, PB003G). PB003 to atrakcyjna koncepcja leku o bardzo silnej przewadze konkurencyjnej w kontekście komercjalizacji na rynku terapii nowotworów.
„W przypadku projektu PB003, podobnie jak w PB004, będziemy starali się uzyskać jak najszersze finansowanie grantowe, tak aby zabezpieczyć ze środków publicznych dużą część funduszy niezbędnych do rozwoju tej potencjalnej nowej terapii. Niezależnie od wszystkiego jednak, w obu projektach zmieniliśmy plan rozwoju tak, aby uwzględniał przeprowadzenie fazy 0” – mówi dr Filip Jeleń.