6 najważniejszych wydarzeń w polskiej biotechnologii 2022 roku
Rejestracje leku w FDA, rekordowa liczba podpisanych umów partneringowych, emisja akcji połączona z wejściem do akcjonariatu polskiej spółki biotechnologicznej inwestora strategicznego, a nawet wezwanie na akcje spółki notowanej na giełdzie. Oto 6 najważniejszych wydarzeń w polskiej biotechnologii 2022 roku.
Rok 2022 obfitował w wiele wydarzeń w polskiej biotechnologii. Pomimo że kursy akcji spółek z sektora generalnie traciły na wartości lub konsolidowały się, to w branży miała miejsce rekordowa liczba ważnych wydarzeń. Oto nasz subiektywny ranking 6 najważniejszych wydarzeń w polskiej biotechnologii 2022, które naszym zdaniem nakazują z optymizmem patrzeć na rok 2023.
REKLAMA
1. Polpharma Biologics rejestruje lek w FDA, czyli pierwszy polski lek biologiczny trafi do amerykańskich pacjentów
W połowie 2022 roku Amerykańska Agencja ds. Żywności i Leków FDA zarejestrowała opracowany w ramach spółki joint venture pomiędzy Polpharma Biologics i Santo Holding (Grupa Strüngmann) – Bioeq CIMERLI™ lek biopodobny do leku Lucentis®.
„CIMERLI™ (ranibizumab-eqrn) został dopuszczony do leczenia wysiękowej postaci zwyrodnienia plamki żółtej związanego z wiekiem (ang. nAMD) i innymi poważnymi chorobami oka, takimi jak: cukrzycowy obrzęk plamki żółtej (ang. DME), retinopatia cukrzycowa proliferacyjna (ang. PDR), obrzęk plamki w przebiegu zakrzepu naczyń siatkówki (pnia siatkówki żyły środkowej, ang. CRVO i/lub gałęzi siatkówki żyły środkowej, ang. BRVO) oraz neowaskularyzacja naczyniówkowa (ang. CNV). CIMERLI™ jest pierwszym biopodobnym produktem leczniczym zatwierdzonym do leczenia we wszystkich pięciu wskazaniach zarejestrowanych dla leku Lucentis®, który dodatkowo otrzymał status „zastępowalności” (ang. interchangeability). [I] Skuteczność i bezpieczeństwo leku zostały potwierdzone w badaniu III fazy Columbus AMD i okazały się porównywalne z lekiem referencyjnym [II]” - czytamy na stronie Biotechnologia.pl.
To pierwszy polski lek biopodobny zatwierdzony przez FDA. Eksperci Polpharma Biologics uczestniczyli w pracach nad transferem procesu i metod analitycznych oraz ich walidacją. Firmą odpowiedzialną za komercjalizację nowego leku biopodobnego jest Coherus BioSciences, Inc.
Zobacz także: Polpharma Biologics mogłaby być najwyżej wycenianą spółką biotechnologiczną na giełdzie, gdyby była notowana na GPW
2. Komercjalizacja PCR|ONE przez Scope Fluidics
Na początku sierpnia 2022 Scope Fluidics, notowana na rynku NewConnect biotechnologiczna spółka rozwijająca innowacyjne projekty wykorzystujące technologie mikroprzepływowe do zastosowań w diagnostyce molekularnej, sprzedała 100% udziałów w swojej spółce zależnej: Curiosity Diagnostics Sp. z o.o. na rzecz Bio-Rad Laboratories, Inc. (NYSE: BIO i BIOb) za łączną kwotę do 170 mln USD. Cena za udziały wynosi 100 mln USD, a spółka może otrzymać dodatkowo do 70 mln USD w płatnościach warunkowych.
Projekty Scope Fluidics PCR|ONE i Bacteromic
Transakcja jest przełomowa pod wieloma względami. Jej kluczowym efektem jest to, że akcjonariusze Scope Fluidics otrzymają spektakularną dywidendę z komercjalizacji Curiosity Diagnostics, a dalszy rozwój kolejnych projektów spółki będzie rozwijany z zatrzymanej pozostałej części środków z komercjalizacji.
Zobacz także: Scope Fluidics wypłaci akcjonariuszom przynajmniej 230 mln zł. Potencjalna stopa dywidendy wynosi obecnie 41%
3. Partneringi, publiczna oferta akcji Ryvu Therapeutics
W grudniu 2022 roku Ryvu Therapeutics zamknęło największą w historii polskiej biotechnologii publiczną ofertę akcji. Pozyskane przez krakowską spółkę środki były większe niż suma emisji akcji przeprowadzonych przez Captor Therapeutics i Poltreg w 2021 roku oraz nieznacznie większa od rekordowej oferty IPO Celon Pharma z 2016 roku.
Jednym z inwestorów w akcje polskiej spółki okazał się europejski gigant sektora biotechnologicznego BioNTech, który objął akcje o wartości 20 mln euro. Ponadto Ryvu podpisało z BioNTech umowę na współpracę naukową i rozwój agonistów STING, o wartości 876,2 mln euro. W ramach płatności upfront payment niemiecka spółka zapłaciła polskiej kolejne 20 mln euro.
BYLIŚMY W LABORATORIACH RYVU THERAPEUTICS OTO JAK:
— Strefa Inwestorów (@strefainw) December 13, 2022
==> https://t.co/jGYG85j9C6@RyvuTx @przewiezlikowsk #Giełdowaturystyka pic.twitter.com/BqB8b3WV6K
Wcześniej Ryvu Therapeutics podpisało umowę partneringową na projekt z obszaru early pipline, o wartości 400 mln USD. W ramach podpisanej umowy wraz z amerykańską spółką, notowaną na Nasdaq, Exelixis będzie rozwijać technologię celującą w białko STING wraz z koniugatami. Zgodnie z warunkami umowy, Ryvu otrzymało od Exelixis płatność z góry w wysokości 14,04 mln zł (3 mln USD).
Zobacz także: Ryvu Therapeutics podsumowuje publiczną ofertę akcji. BioNTech i Leukemia & Lymphoma Society dołączyły do akcjonariatu polskiej spółki biotechnologicznej
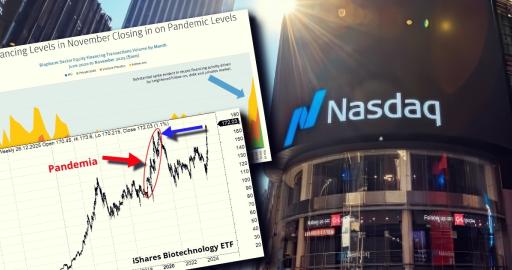
4. Wezwanie na akcje Blirt przez Qiagen
Blirt to notowana na NewConnect spółka z sektora biotechnologicznego, która zajmuje się produkcją enzymów oraz odczynników do badań diagnostycznych. To jeden z podmiotów, który mocno rozwinął się przy okazji wybuchu pandemii, osiągnął znaczące zyski i rozwinął swój portfel produktów. Na początku maja 2022 roku główni akcjonariusze spółki zawarli umowy sprzedaży wszystkich posiadanych akcji, stanowiących 92,1% udziału w kapitale za prawie 263 mln zł. Stroną kupującą okazał się zagraniczny inwestor branżowy Qiagen, który dostarcza rozwiązania dla ponad 500 tys. klientów w zakresie diagnostyki molekularnej, badań i farmacji. To pierwsza w historii polskiej biotechnologii transakcja zdjęcia z rynku giełdowego polskiej spółki biotechnologicznej przez inwestora branżowego głównie ze względu na przejęcie wypracowanej przez polską spółkę technologii i kompetencji.
5. Captor Therapeutics podpisuje współpracę badawczą z Ono Pharmaceutical
W połowie listopada br. Captor Therapeutics zawarł z japońską spółką biotechnologiczną Ono Pharmaceutical umowę o współpracy w zakresie rozwoju małych cząsteczek zdolnych do degradacji ustalonego przez obie strony celu molekularnego, który może mieć zastosowanie przede wszystkim w zakresie chorób neurodegeneracyjnych. Przewidywana maksymalna kwota skumulowanych płatności Ono w ramach podpisanej umowy na rzecz Captor Therapeutics wynosi około 197 mln euro.
Umowa zakłada, że Captor będzie odpowiedzialny za opracowanie kandydata na lek typu degrader małocząsteczkowy, przy wykorzystaniu rozwijanej platformy OptigradeTM, natomiast Ono otrzyma wyłączne prawo do licencji na dalszy rozwój i komercjalizację kandydata na lek.
Podpisana w listopadzie umowa jest o tyle istotna, że może stanowić wskazówkę odnośnie potencjalnej kwoty za komercjalizację projektów własnych spółki, które już w 2023 roku powinny trafiać do fazy klinicznej.
Zobacz także: „Umowa z ONO wzmacnia naszą pozycję w oczach największych graczy przemysłu farmaceutycznego” - relacja czatu z zarządem Captor Therapeutics
6. Molecure rozwiązuje współpracę Galapagos
Pod koniec czerwca 2022 br. Molecure (dawne OncoArendi), odzyskało wszystkie prawa do cząsteczki OATD-01, która była przedmiotem transakcji partneringowej z Galapagos w 2020 roku. Trudno określić jednoznacznie, czy jest to negatywna czy pozytywna informacja.
Decyzja o zwrocie przez Galapagos nieodpłatnie wszystkich praw do OATD-01 to efekt zmiany strategii europejskiej spółki. W Galapagos zmienił się zarząd, a spółka postanowiła skupić się na rozwoju leków onkologicznych. W tym kontekście, pomimo znacznego zaawansowania, projekt polskiej spółki przestał pasować do jej pipeline-u. To pierwsze tego rodzaju wydarzenie w historii polskiej biotechnologii.
Molecure odzyskało pełne i wyłączne prawa do cząsteczki, związane z nią dane, prawa własności intelektualnej oraz wytworzoną substancję aktywną i tabletki. Ponadto do spółki wróciły wyniki wszystkich badań, w tym z rozwoju przedklinicznego i klinicznego OATD-01, które były prowadzone przez Galapagos w ciągu ostatnich 18 miesięcy.
Polska firma biotechnologiczna zatrzyma też kwotę 27 mln euro, którą otrzymała w listopadzie 2020 roku jako część umowy licencyjnej. Wesprze ona finansowanie dalszego badania klinicznego II fazy OATD-01.